CDL(中国糖尿病肝脏病共管行动计划)文献月评——2023年12月第十一期
—— 作者: 时间:2023-12-17
阅读数:
41
前言
糖尿病和肝脏病是我国常见的慢性病,二者在发病机制、临床表现、诊疗靶点等多方面存在着相互作用或互为危险因素,共同管理有利于减轻疾病负担。为助力我国糖尿病肝脏病共管事业发展,本刊携手中国糖尿病肝脏病共管行动计划(CDL)联合推出CDL文献月评专栏,每月分享有关于糖尿病合并肝脏病的疾病机制研究、诊疗进展等相关文献,并邀请国内相关领域的专家进行文献点评,希望为相关领域专家、研究人员及一线医务工作者开展科学研究和临床诊治提供一定的思路和帮助。
本期CDL文献月评将分享糖尿病及脂肪肝相关的6篇基础或临床研究文献。本期特邀点评专家:山东大学第二医院李涛教授,四川大学华西医院吴东波教授,上海交通大学医学院附属瑞金医院陈立教授。

点评专家

李涛教授
山东大学第二医院
山东大学第二医院感染性疾病科/肝病科副主任。山东大学临床副教授、硕士生导师。目前任中华医学会感染病学分会青年委员,中华医学会肝病学分会肝病基础医学与实验诊断协作组委员,山东省医学会感染病学分会副主任委员、青年学组组长,山东省医学会肝病学分会委员、病毒性肝炎学组副组长。
01
成纤维细胞生长因子21通过调节L-乳酸稳态,在1型糖尿病小鼠模型中保护肝脏免受细胞凋亡
Fibroblast growth factor 21 protects the liver from apoptosis in a type 1 diabetes mouse model via regulating L-lactate homeostasis
Yan J, Xie J, Xu S, et al. Biomed Pharmacother. 2023; 168:115737.
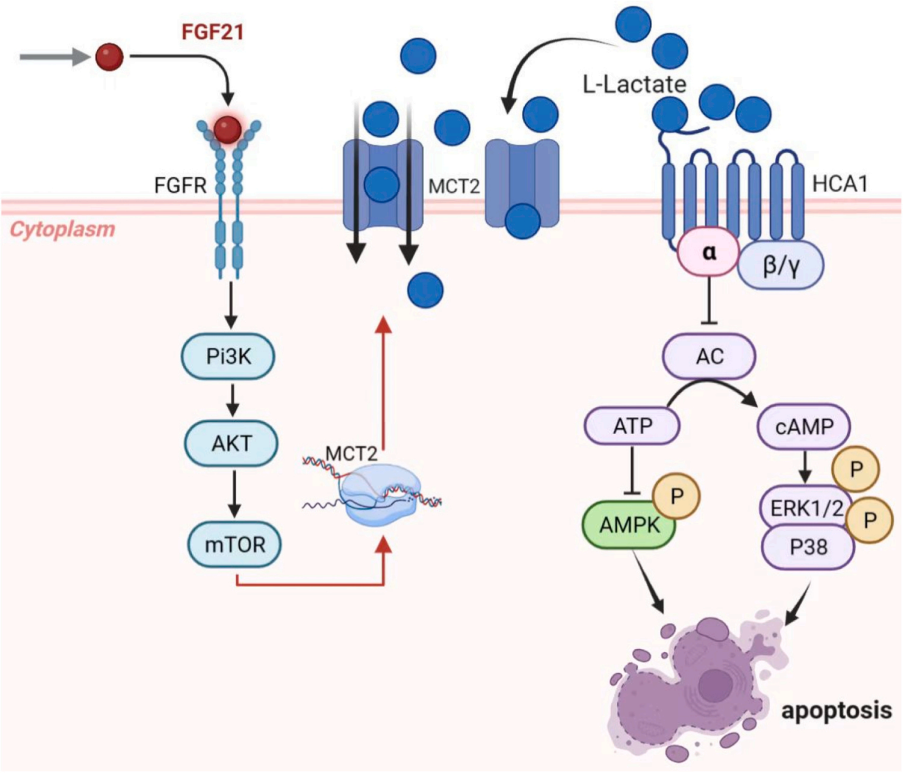
(引自Biomed Pharmacother)
成纤维细胞生长因子21(Fibroblast growth factor 21,FGF21)是一种肝细胞分泌的细胞因子,对葡萄糖和脂质代谢平衡具有多效性作用。本研究的目的是阐明FGF21对1型糖尿病 (type 1 diabetes mellitus,T1DM)小鼠模型中L-乳酸代谢和肝脏损伤的保护作用及机制。结果表明,L-乳酸稳态可能是T1DM相关肝功能异常的治疗靶点。FGF21对肝损伤的保护作用与其改善单羧酸转运蛋白2(MCT2)依赖的Cori循环以及拮抗羟基羧酸受体1(HCA1)介导的ERK1/2、p38 MAPK和AMPK信号传导通路抑制相关。
研究将六周龄雄性C57BL/6小鼠分为对照组、T1DM组/L-乳酸暴露组和FGF21治疗TIDM组/FGF21治疗L-乳酸暴露组。检测T1DM或长期暴露于L-乳酸的野生型和羟基羧酸受体1(HCA1)敲除小鼠的肝细胞凋亡信号传导通路和功能指标。对肝AML12细胞进行高葡萄糖或L-乳酸处理后,检测L-乳酸摄取、细胞凋亡和单羧酸转运蛋白2(MCT2)的表达。在T1DM小鼠模型中,高葡萄糖作用第13周,肝脏FGF21表达下调约1.5倍。外源性给予1型糖尿病小鼠或L-乳酸暴露小鼠FGF21(2 mg/kg)可通过激活细胞外信号调节激酶(ERK)1/2、p38丝裂原激活蛋白激酶(MAPK)和AMP激活蛋白激酶(AMPK)途径显著抑制肝脏氧化应激和细胞凋亡。HCA1-KO小鼠对由糖尿病和L-乳酸引起的肝细胞凋亡和功能障碍具有较低的易感性。此外,抑制PI3K-mTOR的活性表明,FGF21通过上调MCT2蛋白翻译来抑制L-乳酸诱导的Cori循环改变和肝细胞凋亡发挥肝细胞保护作用。
点评
糖尿病与非酒精性脂肪性肝病(NAFLD)联系非常密切。据统计,1型及2型糖尿病患者中NAFLD的患病率分别可达40%~50%及50%~70%。不同于2型糖尿病患者,目前1型糖尿病患者肝损害的病因、发病机制等方面研究较少。
作为一种由禁食或应激诱导的内分泌激素,FGF21广泛参与糖脂代谢。该研究团队在既往研究基础上,重点研究了FGF21对1型糖尿病所致肝脏损伤的保护机制,提示L-乳酸体内稳态有望成为1型糖尿病相关肝脏损伤的潜在治疗靶点。
该研究仍存在一定的局限性。首先,用于干预的FGF21剂量及疗程仍需进一步探索(研究中为2 mg/kg*4周)。其次,目前已有研究证实在多个组织中β-klotho/FGF受体复合物可调节FGF21的功能,并有研究称β-klotho蛋白可以刺激星形胶质细胞形成和释放L-乳酸,因此,需要进一步的研究探索β-klotho对肝脏L-乳酸摄取是否存在影响。再者,该研究缺乏T1DM小鼠肝脏中胞外L-乳酸积累的直接体内证据。最后,由于缺乏接受FGF21的正常小鼠实验组,该研究无法确定FGF21对正常肝代谢的影响。
02
有氧运动引起的chemerin减少通过调控关键代谢酶和蛋白质改善糖尿病小鼠的糖脂代谢紊乱和脂肪肝
Aerobic exercise-induced decrease of chemerin improved glucose and lipid metabolism and fatty liver of diabetes mice through key metabolism enzymes and proteins
Lin X, Qu J, Yin L, Wang R, Wang X. Biochim Biophys Acta Mol Cell Biol Lipids. 2023;1868(12):159409.
既往研究表明,脂肪因子chemerin在运动改善糖脂代谢和糖尿病大鼠脂肪肝病变中发挥重要作用,但其潜在的机制尚不清楚。本研究首次采用外源性chemerin补充剂来探究运动后chemerin下降在糖尿病小鼠的作用,以及其对糖脂代谢关键酶的调控作用,如脂肪甘油三酯脂肪酶(ATGL)、脂蛋白脂肪酶(LPL)、磷酸烯醇丙酮酸羧激酶(PEPCK)和葡萄糖转运蛋白4 (GLUT4)。
研究建立了两种脂肪特异性chemerin基因敲除小鼠模型,以研究chemerin对葡萄糖及脂质代谢酶的调节作用。研究发现,在糖尿病小鼠中,运动能够改善糖脂代谢和脂肪肝,并通过调节肝脏、腓肠肌和脂肪组织中ATGL、LPL和GLUT4等关键酶来实现。然而,外源性补充chemerin可以逆转这种改善作用。此外,在chemerin敲除小鼠中,chemerin(-/-)?adiponectin小鼠的体脂量较低,血糖和血脂得到改善,且不会发生脂肪肝;而chemerin(-/-)?fabp4小鼠则存在高脂血症且体脂量没有得到改善。尽管两种chemerin(-/-)小鼠的脂肪过氧化物酶体增殖激活受体γ(PPARγ)、ATGL、LPL和GLUT4增加,但肝脏和腓肠肌中的PPARγ、ATGL、LPL、GLUT4和PEPCK在chemerin(-/-)?adiponectin小鼠中得到改善,而在chemerin(-/-)?fabp4小鼠中则恶化。由此可见,chemerin的减少在运动引起的糖尿病小鼠糖脂代谢和脂肪肝改善中发挥重要作用,这可能是通过PPARγ介导外周代谢器官中ATGL、LPL和GLUT4的升高而实现的。
点评
众所周知,有氧运动对于预防和治疗肥胖及其相关疾病具有重要作用,但其相关机制目前仍需进一步探索。Chemerin主要在肝脏和脂肪细胞中产生,具有脂肪因子和趋化因子的特性。有研究已经发现运动可以诱导脂肪因子chemerin表达下降,从而改善肥胖和糖尿病患者以及正常老年人的糖脂代谢,减轻肝脏炎症。因此,该研究团队在既往研究基础上,应用chemerin基因敲除小鼠模型,聚焦ATGL、LPL和GLUT4等调节糖脂代谢的关键代谢酶和蛋白质,并提示了PPARγ的可能介导机制。当然,PPARγ的调节作用需要进一步研究证实。另外,研究发现无需体重减轻,运动本身即可降低糖尿病小鼠的chemerin水平。
该研究的局限性在于仅研究了接受高脂饮食的chemerin (-/-) 小鼠的糖脂代谢,并未使用STZ构建糖尿病chemerin (-/-) 小鼠模型。相关机制需要未来进一步的研究验证。
点评专家

吴东波教授
四川大学华西医院
博士,临床医学博士后,副教授,硕士研究生导师。中国研究型医院学会分子诊断专委会肝病精准诊断与治疗学组委员、全国疑难及重症肝病攻关协作组委员、四川省医学会感染病学专委会秘书。主持国家自然科学基金青年基金1项、省科技厅课题1项、博士后基金3项。研究兴趣方向:肝脏免疫与肝脏病理,特别是代谢性及免疫性肝病。
03
在新发的2型和1型糖尿病患者中,胰岛素清除率降低与肝脏脂质含量增加和血糖控制不佳存在不同的关系
Reduced Insulin Clearance Differently Relates to Increased Liver Lipid Content and Worse Glycemic Control in Recent-Onset Type 2 and Type 1 Diabetes
Zaharia OP, Antoniou S, Bobrov P, et al. Diabetes Care. 2023;dc231267
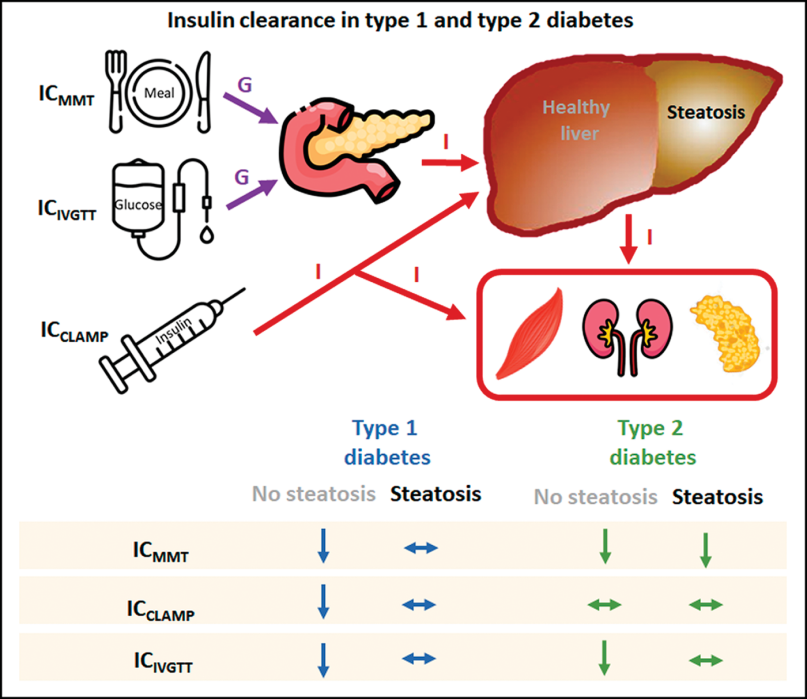
(引自Diabetes Care)
糖尿病可能会导致胰岛素动力学受损,肝脏代谢和血糖调控异常可能会加剧这种情况。因此,本研究探讨了新发糖尿病患者的胰岛素清除率及其可能的影响因素。
研究对象来自于德国糖尿病研究项目的1型糖尿病(T1D)、2型糖尿病(T2D)和正常糖耐量(CON)者各306、489和167例。所有参与者均接受高胰岛素正糖钳夹试验以评估全身胰岛素敏感性(M值)和胰岛素清除(ICCLAMP)。在静脉葡萄糖耐量试验(ICIVGTT)和混合膳食试验(ICMMT)期间进一步计算胰岛素清除率。采用1H-MRS定量评估肝细胞脂质含量。与CON组相比,T1D和T2D组的ICCLAMP(分别为0.12± 0.07和0.21±0.06 比 0.28 ± 0.14,P<0.05)和ICMMT(分别为0.71±0.35 和0.99±0.33 比1.20±0.36,P< 0.05)均较低。在T1D中,ICCLAMP、ICIVGTT和ICMMT与HbA1c呈负相关(P< 0.05)。M 值与CON和T2D中的ICIVGTT呈正相关(r=0.199和r=0.178,P<0.05),与CON中的ICMMT 呈正相关(r=0.176,P<0.05)。肝脏脂质含量与T2D和CON中的ICIVGTT和ICMMT呈负相关(r=-0.005 和 r=-0.037;r=-0.127和r=-0.058,P<0.05)。与此一致,患有脂肪变性的T2D或CON受试者的ICMMT低于那些没有脂肪变性的受试者(P<0.05)。诊断后第一年内,T1D和T2D患者的胰岛素清除率均降低,胰岛素清除率在T2D中与肝脏脂质含量相关,而在T1D中与血糖控制受损相关。胰岛素清除率的差异表明了胰岛素动力学在不同类型糖尿病患者中的特定变化。
点评
胰岛素清除是指机体对血液中胰岛素的去除或降解过程,在糖尿病和代谢性疾病的研究中具有重要的临床价值。既往研究提示,在2型糖尿病中,胰岛素缺乏的病因除了胰腺β细胞退化导致胰岛素分泌减少,也包括胰岛素清除率升高和胰岛素降解能力增加等。胰岛素清除直接反映了机体对胰岛素的生理调控能力。而肝脏是胰岛素清除的主要部位,也是胰岛素发挥代谢调节作用的重要器官。
本研究发现胰岛素清除在新发型1型糖尿病和2型糖尿病患者中降低,进一步揭示了糖尿病发病初期的生理变化。此外,胰岛素清除与肝脏脂肪含量及糖尿病患者的血糖控制水平密切相关,为制定个体化的治疗方案提供了线索。
值得关注的是,胰岛素清除减少是否直接导致肝脂含量增加和血糖控制恶化,或者是否存在其他潜在因素,尚需进一步的研究证实。特别是脂肪肝人群中胰岛素清除率的水平及调控机制有待深入研究。胰岛素清除的研究不仅有助于深化对代谢性疾病病理生理的认识,也为精准医学的实践提供了重要参考。
04
老年人脂肪肝变化是2型糖尿病的重要危险因素:一项全国性队列研究
Fatty Liver Change in Older Adults as an Important Risk Factor for Type 2 Diabetes: A Nationwide Cohort Study
Park KY, Park JH, Han K, et al. Mayo Clin Proc. 2023;S0025-6196(23)00121-0.
为探讨老年糖尿病前期患者脂肪性肝病(FLD)随时间的变化与2型糖尿病发病风险之间的关联,本研究对2009年和2011年接受全国健康筛查的156,984名糖尿病前期老年人进行随访,直至2019年12月31日。其中,FLD的变化根据脂肪肝指数的变化进行分类,糖尿病前期定义为空腹基线血糖水平受损。
研究根据FLD的变化,采用多变量Cox比例风险回归计算2型糖尿病的风险比和CI。在中位8.35年的随访期间,29,422名(18.7%)糖尿病前期的老年人患上了2型糖尿病。与从未患过FLD的患者相比,持续性FLD患者发生2型糖尿病的多变量调整风险比为2.22(95%CI:2.11~2.34)。尽管总体体重减轻5%或更多与所有参与者患2型糖尿病的风险降低7%相关,但脂肪肝状态更重要。即使体重减轻,那些缓解型FLD、新发FLD或持续性FLD病史的人患2型糖尿病的风险也会增加。无论体重变化如何,持续无FLD的个体患2型糖尿病的风险并未增加。
点评
近年来随着人们饮食结构的变化,脂肪肝患病率日益增多。老年脂肪肝是一种在老年人中较为常见的慢性肝脏疾病,常常伴随其他慢性疾病,如2型糖尿病、代谢综合征、高血压、高血脂、高尿酸血症、冠心病等,增加了多重慢性疾病共存的风险。而老年人因生理机能减退,脂肪代谢能力下降,使得脂肪在肝脏沉积的风险增加。越来越多的证据显示脂肪肝与代谢综合征、糖尿病、心血管疾病等疾病的进展密切相关,进一步加重了老年患者的整体健康负担。
本文的研究结果表明,老年人中脂肪肝的发生或变化可能是2型糖尿病的一个重要危险因素。需要注意的是,文章中发现尽管在体重减轻的情况下,那些曾经患有脂肪肝后恢复、新发生脂肪肝,或持续患有脂肪肝的个体,其患2型糖尿病的风险仍有升高。
因此,对于老年脂肪肝患者,应该综合考虑其多重慢性疾病的管理,并通过调整生活方式、饮食习惯等方式,有针对性地预防和控制脂肪肝的发展,以维护老年患者的整体健康。通过关注脂肪肝的变化,或许能够在老年人群体中更好地预防和管理2型糖尿病。
点评专家

陈立教授
上海交通大学医学院附属瑞金医院
上海交通大学医学院附属瑞金医院消化内科,主任医师、副教授、硕士研究生导师。中华医学会肝病学分会青年委员、中华医学会肝病学分会肝炎学组委员、中华医学会肝病学分会肝病相关消化疾病协作组委员、全国疑难及重症肝病攻关协作组委员、上海市中西医结合感染病学会常务委员。长期从事病毒性肝炎和脂肪性肝炎的基础与临床研究,对疑难复杂肝病有丰富的临床诊治经验。主持承担国家自然科学基金2项,在Gut、J Hepatol、PNAS等国内外杂志上发表论著40余篇,担任JCTH,Frontiers系列杂志Editor,作为主要完成人曾获中华医学科技奖、教育部科技进步奖等奖项。
05
FSTL3在2型糖尿病患者中部分介导了非酒精性脂肪性肝病纤维化风险增加与急性心肌梗死的关联
FSTL3 partially mediates the association of increased nonalcoholic fatty liver disease fibrosis risk with acute myocardial infarction in patients with type 2 diabetes mellitus
Duan W, Shi R, Yang F, et al. Cardiovasc Diabetol. 2023;22(1):297.
本研究共纳入1424名参与者,包含429名T2DM患者和995名合并NAFLD的T2DM患者,旨在探讨肝纤维化风险增加与急性心肌梗死(AMI)之间的关联,并探讨血清卵泡抑素样蛋白3(FSTL3)在这种关联中的介导作用。结果表明,T2DM患者中,NAFLD纤维化与AMI密切相关。FSTL3在显著性纤维化和进展期纤维化的NAFLD患者肝脏中表达增强,并且血清FSTL3部分介导了T2DM患者肝纤维化风险增加与AMI的关联。
研究对995名合并NAFLD的T2DM患者,按NAFLD 纤维化风险进行分类,以探讨NAFLD纤维化风险与AMI之间的关联。同时,对60例NAFLD患者进行了肝脏FSTL3的免疫组织化学染色和半定量分析。另外,选取323例合并NAFLD的T2DM患者(191例无AMI,132例AMI)血清样本进行了FSTL3检测,并研究FSTL3在NAFLD纤维化和AMI之间的中介作用。研究发现,NAFLD纤维化风险增加是合并NAFLD的T2DM患者发生AMI的独立危险因素。基因表达综合(GEO)数据库和免疫组织化学染色分析证实,伴有纤维化的NAFLD患者肝脏中FSTL3表达增加。在NAFLD纤维化高风险和AMI患者中,血清FSTL3显著升高,在合并NAFLD的T2DM患者中,血清FSTL3与NAFLD纤维化和AMI严重程度密切相关。最重要的是,分析表明在合并NAFLD的T2DM患者中,血清FSTL3 升高部分介导了NAFLD纤维化风险增加与AMI之间的关联。
点评
血管疾病(CVD)是2型糖尿病最常见的并发症之一,CVD风险受到许多因素的影响。当2型糖尿病合并NAFLD时,CVD风险是否会增加,其内在的关联因子是什么?本研究从人群队列出发,比较了不同NAFLD纤维化阶段急性心肌梗死(AMI)的差异,并探讨了血清卵泡抑素样蛋白3(FSTL3)在AMI中的作用。
研究结果认为随着肝纤维化的增加,合并T2DM的脂肪肝患者AMI风险也随之增加,且血清和肝脏FSTL3表达也随着肝纤维化的程度的增加而增加,故作者推论血清FSTL3 升高部分介导了NAFLD纤维化风险增加与AMI之间的关联。
值得注意的是,在合并脂肪肝的T2DM患者与不合并脂肪肝的T2DM患者之间比较,AMI的发生率并没有差异(32.7% vs. 33.1%,P=0.872),logistics回归分析显示脂肪肝并不是发生AMI的独立危险因素;而AMI的发生率之所以会在不同的肝纤维化级别之间有显著差异,不应忽视年龄在肝纤维化发展中的重要作用。实际上,如本文表2指出,AMI高危人群的年龄明显高于低危人群(P<0.001)。FSTL3是一种脂肪内分泌因子,主要与转化生长因子β(TGF-β)超家族成员如激活素A和肌肉生长抑制素结合,抑制其生物活性,可以解释FSTL3水平与肝纤维化水平呈正相关,也可以在统计学上得出与AMI风险相关。然而,要证明FSTL3介导NAFLD纤维化风险增加与AMI之间的关联仍需要更多的证据。
06
非奈利酮对2型糖尿病、慢性肾病和改变肝脂肪变性和纤维化标志物患者的疗效:FIDELITY亚组分析
Efficacy of finerenone in patients with type 2 diabetes, chronic kidney disease and altered markers of liver steatosis and fibrosis: A FIDELITY subgroup analysis
Perakakis N, Bornstein SR, Birkenfeld AL, et al. Diabetes Obes Metab. 2023;10.
为研究非奈利酮对慢性肾病和2型糖尿病患者的肝功能、心血管和肾脏综合结局的影响,并根据肝脂肪变性、炎症和纤维化风险进行分层。德国科学家就FIDELITY研究进行亚组分析。结果表明,非奈利酮对慢性肾病和2型糖尿病患者的肝功能参数没有影响。非奈利酮在肝功能异常的患者中显示出强大且一致的肾脏保护作用,甚至在纤维化4指数(FIB-4)评分较高且发生心血管并发症风险较高的患者中也显示出心血管保护作用。
研究根据肝纤维化和肝酶水平对患者进行分层,高脂肪肝风险组(肝脂肪变性指数>36);转氨酶升高组(男性ALT >33,女性ALT>25 IU/L)以及FIB-4分层组(FIB-4得分>3.25、>2.67和>1.30)。复合肾脏结局定义为肾衰竭发作、肾小球滤过率比基线下降≥57%,持续时间≥4周或肾功能衰竭死亡。复合心血管结局定义为心血管死亡、非致命性心肌梗死、非致命性中风或因心力衰竭住院。ALT、AST和GGT在治疗组和安慰剂组之间保持一致,并始终保持稳定。非奈利酮可降低复合肾脏结局的风险,与肝功能是否异常无关。FIB-4评分越高,复合心血管结局发生率越高。与安慰剂相比,非奈利酮在FIB-4亚组中分别降低52%(>3.25)、39%(>2.67)和24%(>1.30)的复合心血管结局的发生风险。
点评
非奈利酮是一种非甾体类、选择性盐皮质激素受体(MR)拮抗剂。MR在肾脏、心脏和血管中均有表达,非奈利酮可减轻MR过度激活介导的炎症和纤维化。该药为2型糖尿病相关的慢性肾脏病成人患者提供了新的治疗选择。本研究是一项针对非奈利酮临床试验FIDELITY的亚组分析,旨在评估非奈利酮对伴有肝脂肪变、转氨酶和纤维化标志物升高患者的临床益处,包括对肾脏和心血管的获益。结果显示,首先,非奈利酮对伴有2型糖尿病的CKD患者的肝脏转氨酶没有影响。其次,转氨酶升高或肝纤维化指数升高未改变非奈利酮对复合肾脏结局的影响。在复合肾脏结局中,随着时间推移,与安慰剂相比,非奈利酮始终降低了相对于基线的尿白蛋白/肌酐比值(UACR),并且改善了肝损伤亚组的肾脏结局。第三,高FIB-4评分与较高的CVD并发症风险相关,而非奈利酮显著降低了CVD风险。该研究表明非奈利酮可显著降低合并肝损伤的2 型糖尿病相关的慢性肾脏病成人患者的肾脏和心血管事件发生风险,且对肝脏安全性良好。
*主编:李婕、祁小龙
*执行编辑:杨玥 芮法娟 吉晓蓉

声明:本文仅供医疗卫生专业人士了解最新医药资讯参考使用,不代表本平台观点。该信息不能以任何方式取代专业的医疗指导,也不应被视为诊疗建议,如果该信息被用于资讯以外的目的,本站及作者不承担相关责任。
标签:
研究
热点聚焦
其他肝病
发表评论
全部评论
